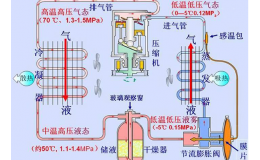
(1)無色液體,有成味,無毒,加入路酸鋰后溶液呈流黃色。
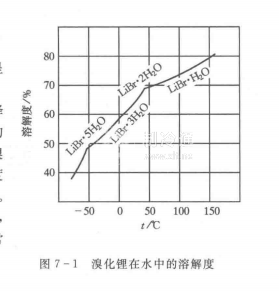
(2)溴化鋰在水中的溶解度隨溫度的降低而降低,如圖7一1所示。圖中的曲線為結晶線,曲線上的點表示溶液處于飽和狀態(tài),它的左上方表示有固體溴化鋰結品析出,右下方表示溶液中沒有結晶。溶解度是指飽和液體中所含溴化鋰無水化合物的質量分數。
由圖中曲線可知,溴化鋰的質量分數不宜超過66%,否則溶液溫度降低時有結品析出,破壞制冷機的正常運行。
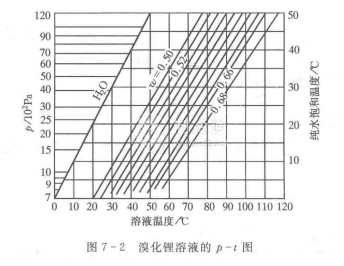
(3)有強烈的吸濕性。液體與蒸氣之間的平衡屬于動平衡,此時分子穿過液體表面到蒸氣中去的速事等于分子從蒸氣中回到液體內的速率。因為澳化鋰溶液中溴化鋰分子對水分子的吸引力比水分子之間的吸引力強,也因為在單位液體容積內溴化鋰分子的存在面使水分子的數日減少,所以在相同溫度的條件下,液面上單位蒸氣容積內水分子的數目比純水表面上水分子數目少。由于溴化鋰的沸點很高,在使用的溫度范圍內不會揮發(fā),因此和溶液處于平衡狀態(tài)的蒸氣總壓力等于水蒸氣的壓力,從面可知溫度相等時:溴化鋰溶液液而上的水蒸氣分壓力小于純水的飽和蒸氣壓力,且濃度愈高或溫度愈低時水蒸氣的分壓力愈低。圖7一2表示溴化捏溶液的溫度,溴化鋰的質量分數與壓力之間的關系。由圖可知,當w為50%,溫度為25℃時,飽和蒸氣壓力為0.85kPa,而水在同樣溫度下的飽和蒸氣壓力為3.167kPa。如果水的飽和蒸氣壓力大于0.85kPa,例如壓力為1kPa(相當于飽和溫度為7℃)時,上述溴化鋰溶液就具有吸收它的能力,也就是說溴化鋰水溶液具有吸收溫度比它低的水蒸氣的能力,這一點正是溴化鋰吸收式制冷機的機理之一,同理,如果壓力相同,溶液的飽和福度一定大于水的飽和溫度,由溶液中產生的水蒸氣總是處于過熱狀態(tài)。
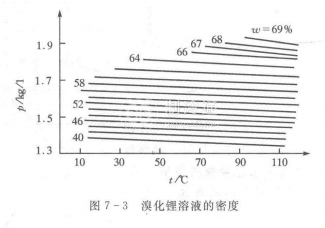
(4)密度比水大,并隨溶液的濃度和溫度而變,如圖7一3所示。
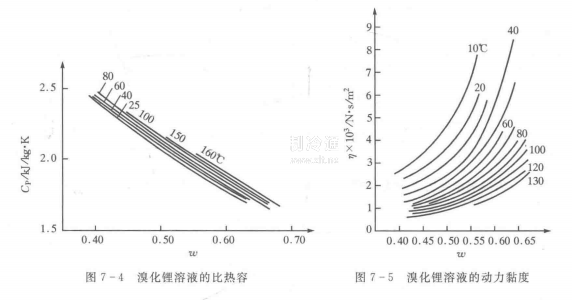
(5)比熱容較小,如圖7-4所示。當溫度為150℃,w為55%時,其比熱容約為2kJ/(kg·K),這意味著發(fā)生過程中加給溶液的熱量比較少,再加上水的蒸發(fā)汽化熱比較大這一特點,使機組其有較高的性能系數
(6)黏度較大。圖7-5示出溴化鋰溶液的動力黏度隨溴化恒的質量分數和溫度的變化關系,例如w為60%,溫度為40℃時,其黏度為6.004×10N·s/㎡(6.12×10-kg·s/㎡),面水在40℃時姑度為6.53×10N·s/㎡(6.66×10kg·s/㎡),
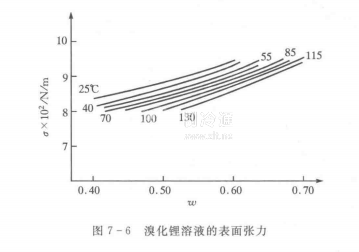
(7)表而張力較大,圖7-6示出溴化鋰溶液的表面張力隨溴化鋰的質量分數和溫度的變化關系。例如w為60%,溫度為40℃時,表面張力為6.96×10N/m.
(8》溴化鋰水溶液的導熱系數隨田之增大面降低,隨溫度的升高而增大。
(9》對黑色金屬和紫銅等材料有強烈的腐蝕性,有空氣存在時更為嚴重。因腐蝕面產生的不凝性氣體對裝置的制冷量影響很大。